서론
안녕하세요, 건강과 학술정보를 제공하는 KRHOW입니다. 오늘은 우리 몸 속에 숨겨진 놀라운 미생물 군집, 특히 장내 미생물군이 간에 미치는 영향에 대해 이야기해보려고 합니다. 많은 분들이 이미 장내 미생물군이 우리 건강에 중요한 역할을 한다는 것을 알고 계시겠지만, 이번 연구를 통해 알아본 새로운 사실들은 그 중요성을 다시 한번 일깨워줍니다. 소중한 시간 내주셔서 감사합니다. 지금부터 흥미롭고 유익한 정보를 제공해드리겠습니다.
전문가에게 상담하기
이 글은 TS.BS Nguyen Khanh Hoa – 연구 프로젝트 관리자, Vinmec 줄기 세포 및 유전자 기술 연구소의 자료를 기반으로 합니다. 믿을 만한 전문가들의 연구 결과를 통해 여러분께 정확하고 깊이 있는 정보를 제공해드리고자 합니다.
장내 미생물군이 간에 미치는 영향: 연구 결과
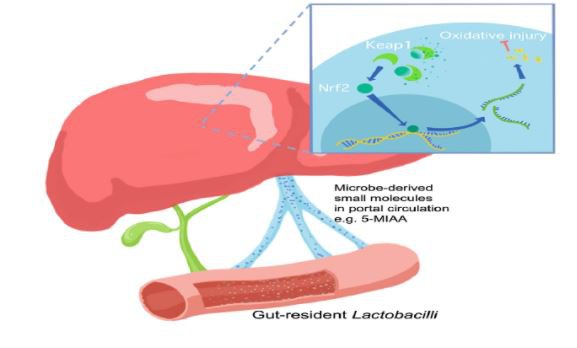
이번 연구에서는 장내 미생물군이 간의 항산화 반응을 유도하고 산화성 간 손상 보호에 기여한다는 사실이 밝혀졌습니다. Saeedi et al. 연구팀은 장내 미생물들이 장 밖의 기관, 특히 간에 어떻게 영향을 미치는지에 대해 상세히 조사했습니다. 그 결과, 장내 유산균이 간의 항산화 시스템을 활성화하고 외인성 유산균 투여가 산화성 간 손상 방지에 효과적임을 확인했습니다.
연구의 중요성과 배경
장내 미생물군이 건강에 미치는 큰 영향은 이미 여러 연구에서 밝혀졌지만, 구체적인 작용 메커니즘은 여전히 미지의 영역이었습니다. 이번 연구에서는 무균 조건에서 사육된 쥐의 간 대사 연구를 통해 Nrf2 항산화제 및 생체 내 반응의 상향 조절을 밝혔습니다. 또한 유산균속의 특정 박테리아, 특히 Lactobacillus rhamnosus GG (LGG)가 Nrf2를 자극할 수 있는 능력을 가진다는 사실도 입증되었습니다.
장내 미생물군의 역할
우리 장에는 약 100조 개 이상의 박테리아와 여러 곰팡이, 바이러스가 공존하고 있습니다. 이러한 미생물들은 장에서 작용할 뿐만 아니라 간, 땀샘, 췌장, 심장, 뇌 등 여러 장기의 기능에도 영향을 미칠 수 있습니다.
간은 특히 중요한 역할을 합니다. 장에서 소화된 물질들은 간으로 운반되어 해독 과정을 거치게 됩니다. 간은 다양한 외인성 물질과 생체 이물 사이의 경계에서 중요한 보호 기능을 합니다. 여러 수용체들이 생체 이물의 존재를 감지하고 적절한 세포 반응을 조절합니다. 최근 연구에 따르면 이러한 수용체들은 장내 미생물에서 유래한 펩타이드 및 소분자에 의해 변경될 수도 있습니다.
연구 결과의 의의
이번 연구에서는 무균 조건에서 사육된 쥐와 박테리아에 노출된 쥐를 비교하여 간 대사의 차이를 발견했습니다. 특히 간 아미노산 대사, 담즙산 생합성 및 요소 순환 경로가 미생물군집에 의해 변경되었습니다. 이러한 분석은 약물 대사 및 항산화 반응과 관련된 네트워크 네트워크를 보여주었습니다.
장내 미생물군의 다른 장기 영향과 관련된 연구
연구팀은 초파리를 모델로 사용하여 Lactobacillus속의 특정 구성원이 전신 Nrf2 활성화를 유도할 수 있음을 발견했습니다. Lactobacillus rhamnosus GG(LGG)의 경구 투여는 정상 쥐의 간에서 Nrf2 신호를 활성화시켰고, 이는 두 가지 다른 급성 산화성 간 손상 모델로부터 보호할 수 있었습니다. 또한 LGG 처리가된 마우스에서 5-메톡시인돌아세트산(5-MIAA)이 간 Nrf2를 활성화할 수 있는 새로운 LGG 유래 저분자임을 확인했습니다.
결론 및 제언
결론
이 연구 결과는 미생물군집-장-간 축의 기능적 관계에 대한 우리의 이해를 크게 확장시켰습니다. 특히 Lactobacillus rhamnosus GG가 간에서 Nrf2 신호 전달 경로를 촉진함으로써 간 손상을 방지할 수 있는지를 입증했습니다. 이러한 발견은 미생물군이 단순한 장 건강을 넘어, 다른 주요 장기의 보호와 치료에도 중요한 역할을 할 수 있음을 시사합니다.
제언
현재의 지식을 기반으로 한 구체적인 권장 사항은, Lactobacillus rhamnosus GG를 포함한 유산균의 섭취가 간 건강에 미치는 긍정적인 효과를 강화할 수 있다는 것입니다. 장과 간의 관계를 이해하고 장 건강을 유지하는 것이 중요하며, 이를 위해 규칙적인 유산균 섭취나 프로바이오틱스 보충제를 고려해보는 것도 좋습니다. KRHOW는 여러분의 건강과 복지를 돕기 위해 계속해서 유익한 정보를 제공할 것입니다. 감사합니다.
참고 문헌
이 글은 국제 Vinmec 병원의 웹사이트를 참고했습니다.